La segunda generación de tratamientos para la EM es ya una realidad.
Autor: Dr. Guillermo Izquierdo
Jefe de la Unidad de E.M. del Hospital Virgen Macarena de Sevilla
Presidente del CMA de AEDEM-COCEMFE
Asociación Neuroinvest

En 1992 un estudio mostraba la capacidad de un anticuerpo monoclonal, de impedir que los linfocitos activados cruzasen la barrera hemato-encefálica y entrasen en el sistema nervioso central (SNC). Aunque este trabajo se realizó en la Encefalitis águda experimental (EAE), un modelo animal de Esclerosis Múltiple (EM), la utilidad de este conocimiento de poder evitar el paso de linfocitos activado al SNC de enfermos con EM, no pasó desapercibido para otros investigadores que utilizarían este tratamiento en pacientes con EM. Entre los científicos que firmaban este estudio figuraba un cordobés afincado en Madrid, el Dr Sanchez Madrid, que ha dedicado muchos años de esfuerzo a comprender como se produce la entrada de linfocitos en el sistema nervioso central (SNC). Este fue el primer jalón importante en una carrera que ha culminado recientemente en el registro del Tysabri (Natalizumab), para el tratamiento de algunas formas de EM que evolucionan por brotes.
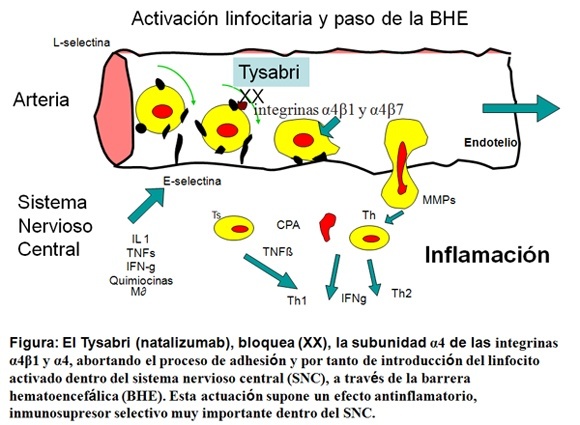
En la EM se produce una inflamación del SNC que se inicia fuera de él, con una activación de los linfocitos que en condiciones fisiológicas, circulan y establecen contacto rodando temporalmente sobre el endotelio vascular del SNC. Estos contactos débiles y transitorios están mediados por moléculas de adhesión de baja afinidad denominadas selectinas, que se expresan en la superficie de las células endoteliales y leucocitos. Estas interacciones de baja afinidad no permiten a los leucocitos detenerse y migrar a través de la BHE hasta que existe una inflamación local en el lugar de interacción entre el leucocito y el endotelio vascular, en ese momento sustancias como las citocinas y las quimiocinas producidas en el foco inflamatorio activan las células endoteliales de las vénulas, lo que promueve la expresión de otras moléculas endoteliales que facilitan la adherencia del linfocito y el endotelio vascular.
Se produce como consecuencia un rodamiento de los leucocitos sobre la pared vascular, lo que reduce su velocidad de desplazamiento y facilita su respuesta a las citoquinas de la superficie endotelial o la luz vascular. Estos hechos permiten a la célula detenerse y comenzar el proceso de migración trans-endotelial.
El natalizumab una molécula, que reconoce y se fija específicamente a una parte de una integrina (la subunidad α4 de las integrinas α4β1 y α4β7), evitando que el efecto fisiológico se produzca. El natalizumab es un anticuerpo monoclonal y como tal se produce a partir de una única línea clonal de células murinas productoras de anticuerpos fusionadas con células tumorales para crear una línea celular híbrida inmortalizada. Los anticuerpos monoclonales murinos desencadenan respuestas inmunes contra ellos cuando se administran a los humanos, por lo que su utilidad terapéutica puede a veces verse limitada por este hecho.
La comercialización de este medicamento no ha estado exenta de problemas, y a pesar de que en los primeros momentos tras la publicación de los resultados positivos del primer ensayo clínico fase II , todo parecía indicar una rápida generalización de su uso, los efectos adversos sin duda relacionados con su gran potencia han hecho que se retrasara y limitará su empleo.
Para que las agencias reguladoras (EMEA en Europa y FDA en Estados Unidos), acepten una indicación terapéutica para un determinado medicamento, éste debe haber demostrado su eficacia y seguridad en ensayos clínicos, aleatorizados contra placebo, diseñados con esta finalidad, que se denominan ensayos de fase III. En el caso del natalizumab, la agencia reguladora de Estados Unidos aprobó su indicación en el tratamiento de la EM cuando se presentaron los resultados del análisis intermedio programado para un año de dos ensayos clínicos controlados en fase III, ambos planificados para disponer de datos a las 54 y 120 semanas, denominados AFFIRM y SENTINEL .
Los dos ensayos presentaban un diseño similar. En el estudio SENTINEL se exigía, además, que el paciente hubiese recibido un tratamiento con interferón β-1a durante esos 12 meses previos y mantuviese actividad clínica. En ambos ensayos se comparó el efecto de administrar una pauta fija de natalizumab (300 mg intravenosos cada cuatro semanas) con el efecto del placebo, pero en el estudio SENTINEL tanto los tratados con natalizumab como los tratados con placebo recibieron además una dosis interferón β-1a (30 μg intramusculares cada semana).
En un análisis intermedio del objetivo primario, en el estudio SENTINEL, cuando se dispuso de los datos de los primeros pacientes evaluados se apreció una disminución relativa frente al grupo placebo en la frecuencia anual de recaídas del 68 y 54%, respectivamente (p < 0,01), que se mantuvo cuando se analizó el total de los datos del primer año (65 y 53%), y al finalizar las 120 semanas del estudio (68 y 55%, p<0,01). La proporción de pacientes libres de recaídas durante los dos años en los estudios AFFIRM y SENTINEL fue del 77 y 54% en el grupo del natalizumab, frente al 56 y 32% en el grupo placebo, respectivamente. Aunque no existen todavía datos comporativos, la eficacia del Tysabri supone un incremento de aproximadamente el 50% sobre los inmunomoduladores actualmente aprobados.
Todos estos datos supusieron una petición de autorización de la comercialización del Tysabri en USA, y se comenzó a tratar la EM de forma regular con este medicamento, pero tres meses después se suspendio el estudio SENTINEL, debido a dos notificaciones de leucoencefalopatía multifocal progresiva (LMP) en pacientes que habían recibido natalizumab, aunque en ambos casos asociado a interferón beta. Estos hechos condujeron, además, a la retirada voluntaria del medicamento por el laboratorio responsable de su comercialización, que había sido autorizada tres meses antes para el tratamiento de la EM sobre la base de los resultados del análisis intermedio de los estudios SENTINEL y AFFIRM. Posteriormente se comunicó otro tercer caso de LMP en un paciente tratado con Tysabri para la enfermedad de Chron.
La LMP es una enfermedad neurológica rara, que era poco conocida por ello y asociada a inmunodepresión, debida a enfermedades previas o a tratamientos que la provocan (iatrogénica). Es una enfermedad considerada irreversible y mortal, aunque recientemente se están intentando terapias para controlarla. La enfermedad es provocada por un virus (JC, antes JVC), que en condiciones normales no produce alteraciones en las personas sanas a pesar de que se detecta frecuentemente en orina y en sangre. El mecanismo de acción del natalizumab, produciendo una inmunodepresión selectiva del SNC, hacía prever esta posibilidad al disminuir las defensas el SNC, lo que facilitaría una proliferación de infecciones previamente controladas.
Aunque el riesgo de LMP es del 1 caso de cada mil y en pacientes que además habían sido tratados con terapia combinada, la necesidad de prevenir posibles efectos adversos en una enfermedad que no es mortal, como la EM ha puesto en evidencia la obligatoriedad de realizar un cuidadoso seguimiento de los pacientes tratados con natalizumab no solo para evitar la LMP, sino otras posibles enfermedades oportunistas que puedan afectar al SNC. En cualquier caso hay que considerar que en formas muy agresivas de EM se están utilizando inmunosupresores como la mitoxantrona y la ciclofosfamida que tienen una toxicidad muy alta.
Los laboratorios Biogen y las autoridades reguladoras han colaborado estrechamente en un proyecto que esta permitiendo volver a utilizar el Tysabri en nuestros enfermos.
La ficha técnica permite tratar a natalizumab como tratamiento modificador de la enfermedad en monoterapia en la EM remitente-recidivante muy activa para los siguientes grupos de pacientes: Pacientes con elevada actividad de la enfermedad a pesar de tratamiento con un interferón beta y también en pacientes con EM remitente recidivante grave de evolución rápida.
Aunque la interpretación de la mayor o menor actividad de los diferentes pacientes puede variar la cantidad de pacientes que puedan ser tratados, es previsible que en los próximos meses asistamos a un rápida aplicación de esta nueva medicación en pacientes que o bien no respondían a la terapéutica convencional con interferón beta, o bien tienen una gran actividad que sus neurólogos consideran excesiva para la terapias actuales menos eficaces.
Los neurólogos tenemos un gran reto para interpretar el aluvión de datos, recomendaciones y limitaciones que tenemos delante, para poder interpretar en cada caso que es lo mas adecuado con cada paciente, y a veces asumir riesgos de los que deben ser conscientes nuestros pacientes. Pero todo esto no debe ser cortapisa para utilizar un nuevo y poderoso tratamiento cuando las condiciones lo requieran y lo permitan.
El Tysabri es una medicación cara, su precio es mayor que el de los inmunomoduladores actualmente en uso, lo que añade otra razón para el control de su utilización, aunque esto no debe suponer una restricción, su empleo si está justificado.
Desde el punto de vista práctico el tratamiento se administra mensualmente por vía intravenosa en perfusiones, similares a las que se les suele indicar a los pacientes cuando tienen brotes, con choques de corticoides,. La administración se debe hacer en hospitales, ya que, aunque solo en ocasionalmente, pueden existir reacciones de hipersensibilidad que requieren atención médica inmediata, en general sin necesidad de que sean ingresados. Precisan permanecer unas horas en un centro sanitario, para lo que se suele utilizar unidades especiales como la Unidad de Día existente en la mayoría de los hospitales.
Este tratamiento es sin duda el primero de una nueva generación que en pocos años nos va a llevar a controlar mucho mejor la EM, sobre todo en los pacientes con mas actividad inflamatoria. Los neurólogos debemos ser prudentes pero a la vez preactivos y aceptar el reto. A los pacientes una vez mas tenemos que pedirles confianza y un poco mas de paciencia, pero les podemos asegurar que sean conscientes de los progresos que en el tratamiento de la EM se han producido en los últimos años, que no son mas que la punta del Iceberg de los que se avecinan.


